Agonistas del receptor de GLP-1 en la diabetes tipo 2
Fecha: 21-03-2018
ISBN: 978-84-15037-74-3
Las acciones pancreáticas de los GLP-1 incluyen la estimulación de la secreción de insulina de forma dependiente a la glucosa y un efecto supresor sobre la secreción de glucagón, responsable de la producción endógena de glucosa. La breve vida media del GLP-1 nativo (menos de 2 minutos) hace impracticable su uso clínico.
Los arGLP1, gracias a diversas modificaciones estructurales, tienen una resistencia significativa al efecto de la enzima que los degrada (la DPP-4), permiten su administración subcutánea y una cobertura que varía desde unas horas a varias semanas. Constituyen uno de los fármacos antihiperglucemiantes de mayor potencia por la reducción de HbA1c, sin riesgo de hipoglucemia. La potencia biológica de los arGLP-1 es 4-6 veces superior a la de los iDPP-41,2.
Los arGLP-1 igualan o superan incluso el tratamiento con insulina basal, y aportan la ventaja adicional de no precisar controles de glucemia capilar con tiras reactivas ni ajustar la dosis en base a los valores de glucemia capilar.
Tipos de agonistas del receptor de GLP-1
Existen diferencias entre los arGLP-1 según el tiempo de acción (tabla 1).
Los de acción más corta y estructura similar al exendina-4 (formulación sintética derivada de un péptido contenido en la saliva del monstruo de Gila) son: exenatida y lixisenatida. Ambos ejercen un efecto más potente sobre la glucemia posprandial al retrasar el vaciamiento gástrico, además de favorecer la secreción de insulina e inhibir el glucagón. Se acompaña de mayor frecuencia de náuseas en las fases iniciales del tratamiento.
Los de acción más prolongada (liraglutida, exenatida semanal y dulaglutida) tienen menor efecto sobre el vaciamiento gástrico, pero son más potentes sobre la glucemia en ayunas. Los arGLP-1 de liberación prolongada se asocian a un aumento de la frecuencia cardíaca, posiblemente por estímulo simpático (o inhibición tono vagal)3.
|
Tabla 1. Tipos de fármacos agonistas del receptor de GLP-1 | ||||
|---|---|---|---|---|
|
Acción prolongada |
Acción corta | |||
|
Una vez al día |
Una vez a la semana |
Dos veces al día |
Una vez al día | |
|
Liraglutida (Victoza©) |
Exenatida LAR (Byetta©) |
Dulaglutida (Trulicity©) |
Exenatida (Byetta©) |
Lixisenatida (Lixumia©) |
|
Monoterapia o terapia combinada con cualquier antidiabético, incluyendo insulina Independiente del IMCa |
Terapia combinada. No indicado en monoterapia. Independiente del IMCa |
|||
|
Predomina efecto sobre glucemia basal |
Predomina efecto sobre glucemia posprandial |
|||
|
Disminuye los eventos CV |
|
|
Seguridad en los eventos CV |
|
|
IMC: índice de masa corporal; CV: cardiovascular. aLa ficha técnica permite prescribir arGLP-1 en pacientes con o sin sobrepeso u obesidad. Pero el visado de inspección en España solo autoriza a prescribirlo en pacientes con IMC > 30 kg/m2. |
||||
Eficacia y seguridad
Los programas clínicos de los diferentes arGLP-1 suman más de 400 ensayos clínicos y 74 metanálisis que avalan la validez de los datos de su eficacia.
Además del beneficio hipoglucemiante, tienen un efecto reductor de peso a diferencia de las sulfonilureas o las glitazonas, que lo incrementan.
Se dispone de seis diferentes moléculas dentro de la familia de los arGLP-1. La albiglutida dejará de comercializarse en junio de 2018, y la semaglutida y la langlenatida están en fase de desarrollo.
La dosis recomendada de exenatida LAR es de 2 mg una vez a la semana. Los pacientes que cambien de exenatida de liberación inmediata (ELI) a la de liberación prolongada pueden experimentar aumentos transitorios de la glucemia, que generalmente mejoran durante las dos primeras semanas después de haber iniciado el tratamiento. La ELI se administra en dosis de 5 μg o 10 μg en cualquier momento dentro de un período de 60 minutos antes de las dos comidas principales del día, separadas por aproximadamente 6 horas o más. No debe ser administrada después de la comida4,5.
La dosis de inicio de la lixisenatida es de 10 μg, una vez al día, durante 14 días. Posteriormente, se continúa con una dosis de mantenimiento de 20 μg/día6. La liraglutida debe iniciarse con 0,6 mg/semana e incrementarse a 1,2 mg/día en dosis única. En función de la respuesta clínica, al menos 1 semana después, es posible aumentar la dosis a 1,8 mg/día7.
La dosis habitual de dulaglutida es de 1,5 mg/semana, aunque en monoterapia y en pacientes mayores de 75 años se recomienda 0,75 mg/semana como dosis inicial8.
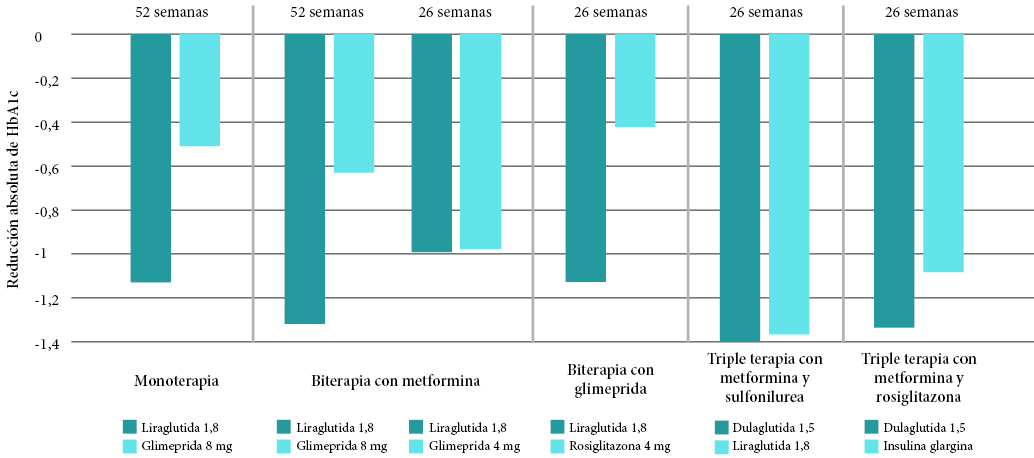
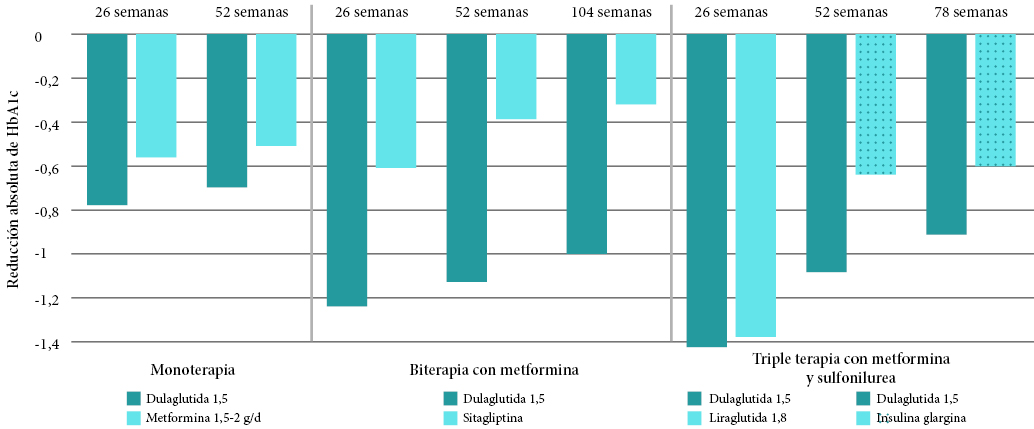
En las figuras 1 y 2 se describe la reducción de HbA1c con arGLP-1 en comparación con otros antidiabéticos. La mayoría de los estudios incluyen pacientes con HbA1c basal entre 8-8,5%. Puede comprobarse que en general las reducciones de HbA1c rondan el 1% o más con liraglutida o dulaglutida.
|
Figura 1. Acción de la liraglutida en la reducción de la hemoglobina glicosilada en comparación con otros antidiabéticos9-14 |
 |
|
Figura 2. Acción de la dulaglutida en la reducción de la hemoglobina glicosilada en comparación con otros antidiabéticos15-18 |
 |
La reducción de la HbA1c con ELI 10 μg/12 h, durante 30 semanas, fue de – 0,89%. En un estudio de 26 semanas, ELI disminuyó los valores de la HbA1c – 1,13%, mientras que la insulina glargina disminuyó los valores en – 1,10%, y la insulina aspártica bifásica en – 0,86%. En otro estudio con pacientes tratados con insulina glargina en el que se comparaba la adición de exenatida o insulina lispro, la reducción fue similar al 1% en ambos casos.
La lixisenatida 20 μg durante 24 semanas en pacientes tratados previamente con metformina alcanzó una reducción de la HbA1c de hasta un – 0-92% en comparación con placebo. Otro estudio en el que se comparó la lixisenatida antes de la comida principal o antes del desayuno durante 24 semanas obtuvo reducciones similares de HbA1c (– 0,65% frente a –0,74%). En pacientes tratados con fármacos orales más insulina glargina, la adición de lixisenatida durante 26 semanas, redujo la HbA1c un – 0,63%, en comparación con la adición de insulina glulisina una vez al día (– 0,58%) o tres veces al día (– 0,84%). Las reducciones de la glucosa plasmática en ayunas (GPA) conseguidas oscilaron entre 7,6 y 21,4 mg/dl, y en relación con la glucosa posprandial (GPP), oscilaron entre 81,2 y 143,3 mg/dl.
El estudio GRADE, cuyo diseño fue publicado en 2013, permitirá conocer en 5.000 pacientes con DM2 de menos de 5 años de duración, tratados previamente con metformina, y con HbA1c 6,8-8,5%, la eficacia comparada entre sulfonilureas, iDPP-4, arGLP-1 o insulina tras un seguimiento de 4,8 años en 37 centros sanitarios de Estados Unidos.
El estudio más reciente publicado (SUSTAIN-7)19, que compara semaglutida 0,5 mg/día y dulaglutida 0,75 mg/día en pacientes con HbA1c inicial media del 8,2%, mostró una reducción significativa de la HbA1c del 1,5% frente al 1,1%, respectivamente. Y con las dosis de semaglutida 1,0 mg y dulaglutida 1,5 mg/día, la disminución significativa de la HbA1c fue del 1,8% frente al 1,4%, respectivamente.
Referencias bibliográficas
Campbell JE, Drucker DJ. Pharmacology, physiology, and mechanisms of incretin hormone action. Cell Metab. 2013;17:819-37.
Drucker DJ. The biology of incretin hormones. Cell Metab. 2006;3:153-65.
Garber AJ. Long-acting glucagon-like peptide 1 receptor agonists: a review of their efficacy and tolerability. Diabetes Care 2011; 34 (Suppl. 2):S279-84.
Ficha técnica de exenatida. Agencia Europea del Medicamento. [Último acceso Marzo 2018.] Accesible en: http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/000698/WC500051845.pdf
Ficha técnica de exenatida-LAR. Agencia Europea del Medicamento. [Último acceso Marzo 2018.] Accesible en: http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/002020/WC500108241.pdf
Ficha técnica de lixixenatida. Agencia Europea del Medicamento. [Último acceso Marzo 2018.] Accesible en: http://ec.europa.eu/health/documents/community-register/2017/20170918138688/anx_138688_es.pdf
Ficha técnica de liraglutida. Agencia Europea del Medicamento. [Último acceso Marzo 2018.] Accesible en:http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/001026/WC500050017.pdf
Ficha técnica de dulaglutida. Agencia Europea del Medicamento. [Último acceso Marzo 2018.] Accesible en: http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/002825/WC500179470.pdf
Bode BW, Testa MA, Magwire M, Hale PM, Hammer M, Blonde L, et al.; LEAD-3 Study Group.
Patient-reported outcomes following treatment with the human GLP-1 analogue liraglutide or glimepiride in monotherapy: results from a randomized controlled trial in patients with type 2 diabetes. Diabetes Obes Metab. 2010 Jul;12(7):604-12.
Buse JB, Sesti G, Schmidt WE, Montanya E, Chang CT, Xu Y, et al.; LiraglutideEffect Action in Diabetes-6 Study Group. Switching to once-daily liraglutide from twice-daily exenatide further improves glycemic control in patients with type 2 diabetes using oral agents. Diabetes Care. 2010 Jun;33(6):1300-3.
García-Hernández P, Arechavaleta-Granell Mdel R, Yamamoto J, Falahati A, González-Gálvez G; Grupo de Investigadores de LEAD-3 en México. [Liraglutide and glimepiride on glycaemic control in type 2 diabetes in the Mexican cohort (LEAD3)]. Rev Med Inst Mex Seguro Soc. 2010 Sep-Oct;48(5):543-8.
Marso SP, Daniels GH, Brown-Frandsen K, Kristensen P, Mann JF, Nauck MA, et al.; LEADER Steering Committee; LEADER Trial Investigators. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2016 Jul 28;375(4):311-22.
Rodbard HW, Buse JB, Woo V, Vilsbøll T, Langbakke IH, Kvist K, et al. Benefits of combination of insulin degludec and liraglutide are independent of baseline glycated haemoglobin level and duration of type 2 diabetes. Diabetes Obes Metab. 2016 Jan;18(1):40-8.
Russell-Jones D, Vaag A, Schmitz O, Sethi BK, Lalic N, Antic S, et al.; Liraglutide Effect and Action in Diabetes 5 (LEAD-5) met+SU Study Group. Liraglutide vs insulin glargine and placebo in combination with metformin and sulfonylurea therapy in type 2 diabetes mellitus (LEAD-5 met+SU): a randomised controlled trial. Diabetologia. 2009 Oct;52(10):2046-55.
Mearns ES, Saulsberry WJ, White CM, Kohn CG, Lemieux S, Sihabout A, et al. Efficacy and safety of antihyperglycaemic drug regimens added to metformin and sulphonylurea therapy in Type 2 diabetes: a network meta-analysis. Diabet Med. 2015 Dec;32(12):1530-40.
Meier JJ. GLP1 receptor agonists for individualized treatment of type 2 diabetes. Nat Rev Endocrinol. 2012;8:728-42.
Nathan DM, Buse JB, Kahn SE, Krause-Steinrauf H, Larkin ME, Staten M, et al.; GRADE Study Research Group. Rationale and design of the glycemia reduction approaches in diabetes: a comparative effectiveness study (GRADE). Diabetes Care. 2013 Aug;36(8):2254-61.
Zhang L, Zhang M, Zhang Y, Tong N. Efficacy and safety of dulaglutide in patients with type 2 diabetes: a meta-analysis and systematic review. Sci Rep. 2016 Jan 8;6:18904. doi: 10.1038/srep18904.
Pratley RE, Aroda VR, Lingvay I, Lúdemann J, Andreassen C, Navarria A, et al., on behalf of Sustain7 investigators. Lancet published online January 31, 2018. Doi .org/10.106/s2213-8587(18)30024-X.
Los contenidos publicados por la Fundación redGDPS son un servicio destinado a los profesionales sanitarios de atención primaria. Los contenidos requieren de una formación especializada para su correcta interpretación. En ningún caso la información proporcionada por Fundación redGDPS reemplazará la relación de los profesionales médicos con los pacientes.
La Fundación redGDPS no promueve ninguna actividad que pueda inducir a la prescripción de marcas comerciales, uso de sistemas de determinación de glucosa o productos dietéticos.